研究内容
ゲノムやエピゲノムのダイナミクス
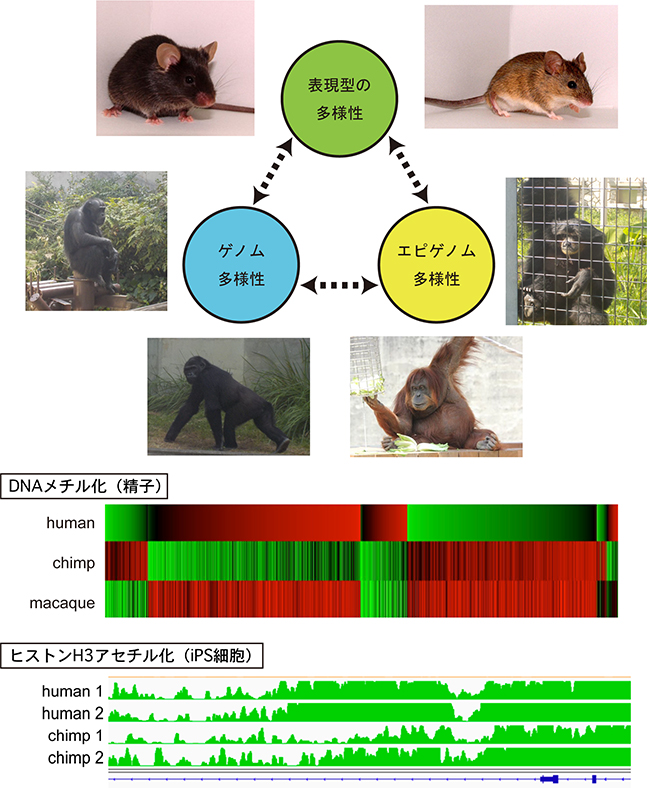
多細胞生物の一個体の中の細胞は基本的にどれも同じゲノム配列を持っていますが、ゲノム配列上に暗号化されている機能は各細胞に適切なゲノム領域だけがデコードされ、細胞固有の性質(遺伝子発現状態)を生み出します。このような制御機構はエピジェネティクスと呼ばれ、主にゲノムDNAとヒストン蛋白質の化学修飾(メチル化など)が関与しています。細胞が持つエピジェネティックな修飾の総体をエピゲノムと呼びます。
エピジェネティックな状態が異なるために個体間で表現型が異なることがあります。私たちの研究室では、エピジェネティックな状態の違いが生み出されるメカニズムは何か、進化の過程でゲノムとエピゲノムはどのように相互作用しながら変化するのかについて研究しています。
具体的には、(1) 種間での違いについてヒト、チンパンジー、ゴリラ、オランウータンなどの霊長類を用いて研究しています。特に、ヒトとチンパンジーのiPS細胞を用いて、細胞分化過程におけるエピゲノムダイナミクスの違いを研究しています。(2)
また、種内でのゲノムやエピゲノムの違いについて、マウス亜種間の比較を行っています。どちらも、解析には主に大規模シーケンサーを用いています。
レトロトランスポゾンの機能と制御
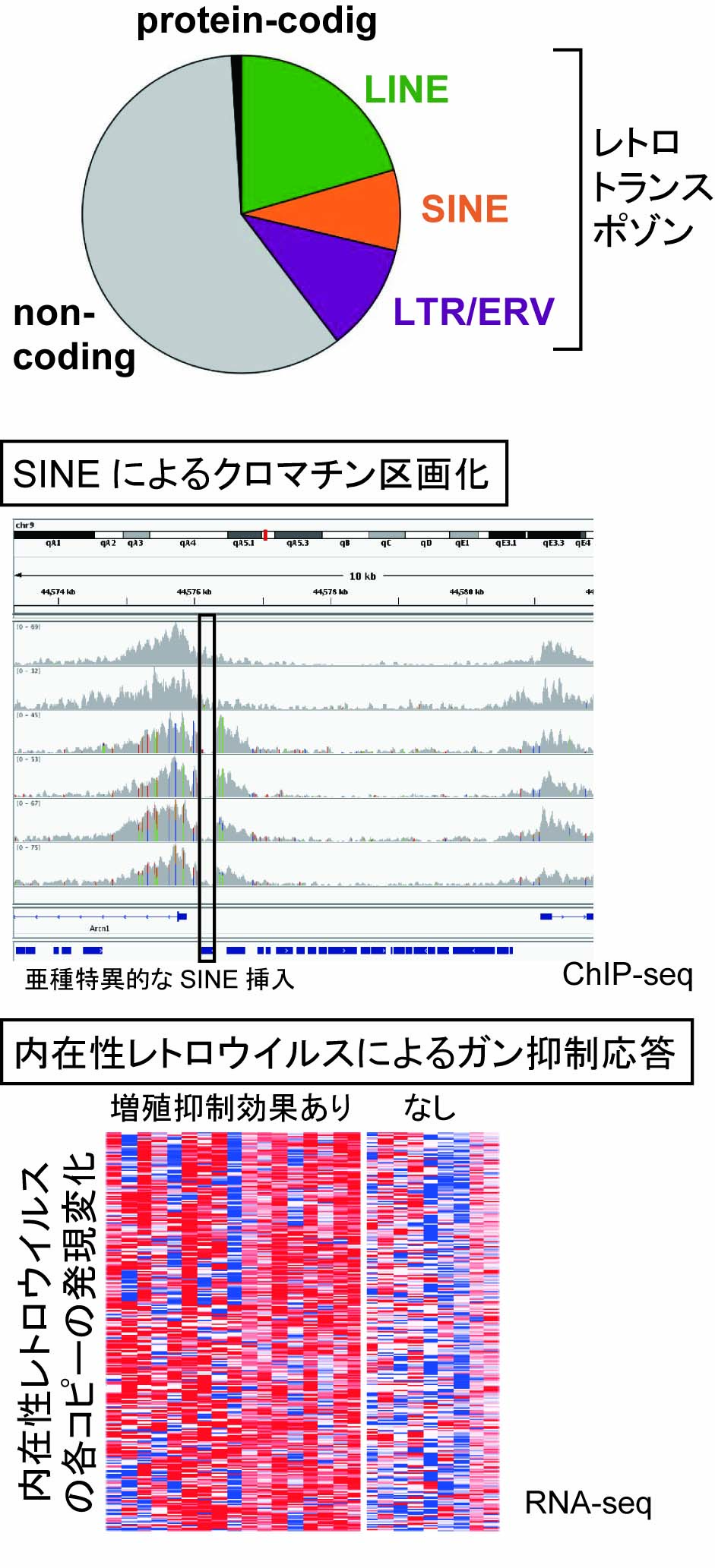
私たちヒトを含め、哺乳類ゲノムで蛋白質をコードしている部分は1%程度しかありません。その他の領域の約半分はレトロトランスポゾンと呼ばれる転移因子によって占められています。
かつて、レトロトランスポゾンはジャンク(がらくた)配列と思われていましたが、今ではゲノム進化の駆動力の一つと考えられています。また、レトロトランスポゾンが他のゲノム領域の機能を制御することも明らかになりつつあります。私たちの研究室では、レトロトランスポゾンにどのような機能があり、その機能はどのように制御されているのか、レトロトランスポゾン転移によってエピゲノムはどういう影響を受けるのかということについて研究しています。
具体的には、(1) SINEレトロトランスポゾンがクロマチンを区画化する現象について、独自に集めたマウス系統間の挿入多型の情報を用いながら、その分子機構を解析を行っています。(2)
抗ガン剤として用いられる5-アザシチジン(DNA脱メチル化剤)の作用機序を調べていくと、ガン細胞ではDNAの低メチル化によって内在性レトロウイルス(ERV)の発現が上昇し、生じたRNAによって自然免疫系が活性化して細胞死に至ることが分かってきました。現在、どのようなヒトERVがどのような機構で自然免疫系の活性化を行うのかを調べています。(3)
最新のエピゲノム編集技術を用いて特定のレトロトランスポゾンファミリーだけをエピジェネティックに活性化し、それによって何が起こるのかを調べています。レトロトランスポゾンの新たな機能の発見を含め、レトロトランスポゾンが大量にゲノムに存在することの意味について、より深い理解を目指しています。
生殖細胞のゲノム安定性とエピゲノム制御
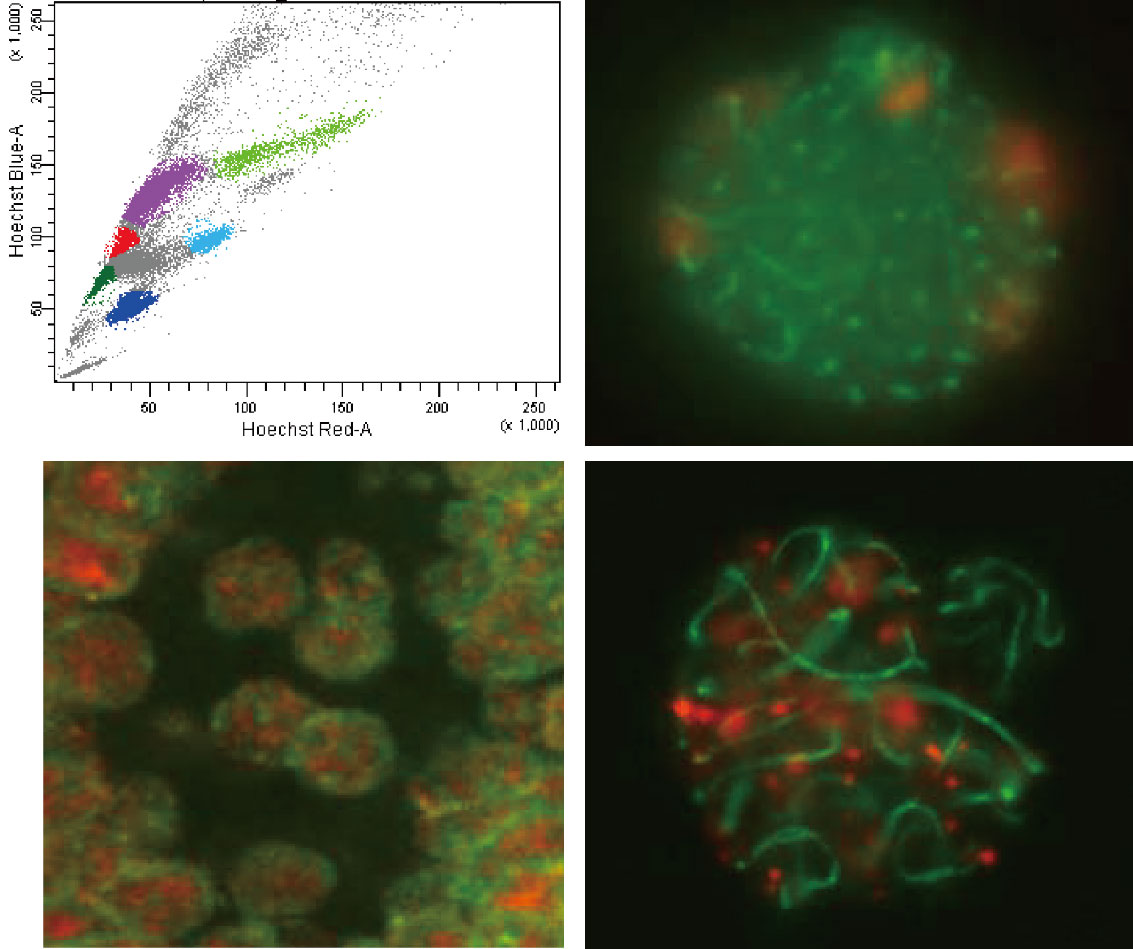
生殖細胞はゲノム情報を次世代に伝える唯一の細胞ですので、レトロトランスポゾンの転移や相同DNA組み換えでの不等交叉などで生じるゲノム配列変化をできるかぎり抑えておく必要があります。私たちの研究室では、生殖細胞の発生過程でレトロトランスポゾンの活性がどのように抑制されているのか、減数分裂期の相同DNA組み換えがどのように制御されているのかについて、エピジェネティクスの観点から研究しています。
世代を超えたエピジェネティックな遺伝の分子機構
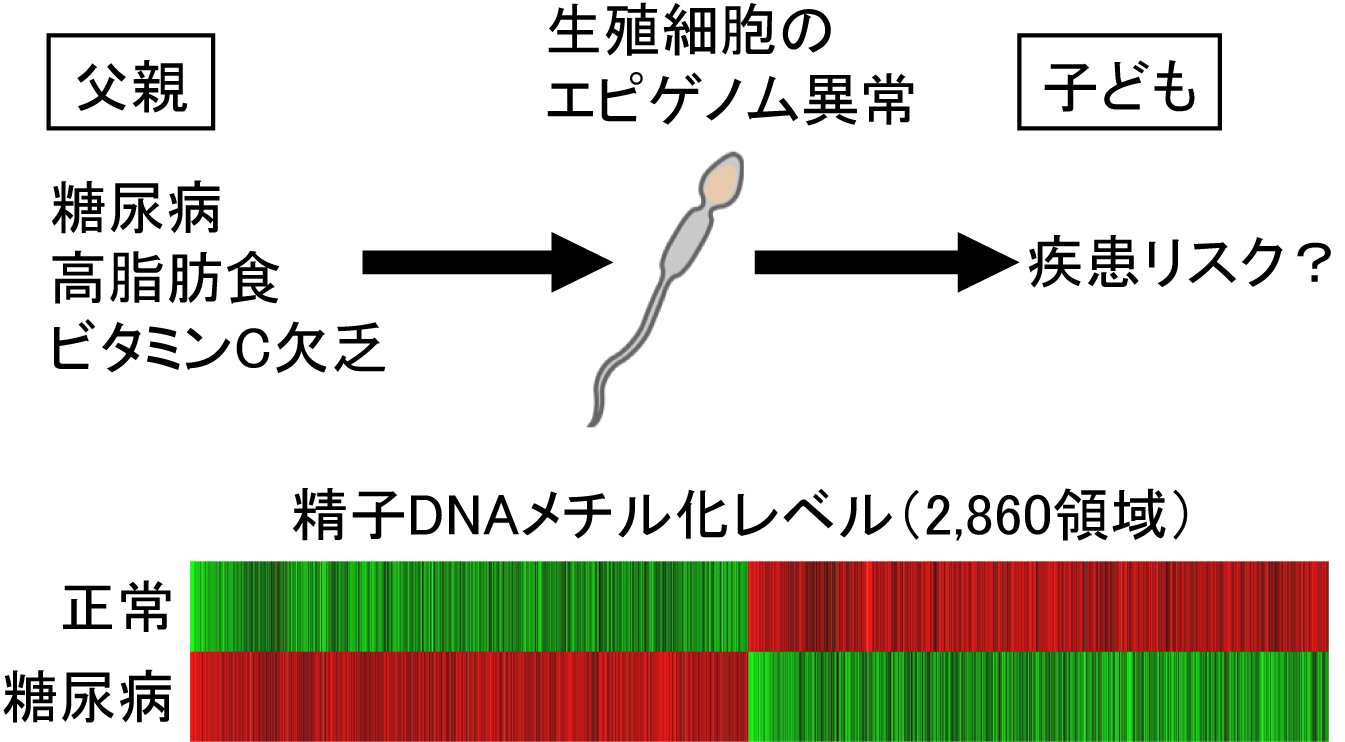
親から子へ形質が遺伝するのは、親と同じ塩基配列をもったDNAを子供が受け取るからです(染色体組み換えと有性生殖により、完全一致ではないです)。しかし、近年、哺乳類において、DNA塩基配列だけでなく他のタイプの遺伝情報も伝えられているのではないかと考えられ始めています。実際、植物ではDNAメチル化状態が子供に遺伝することが知られています。哺乳類でも、同じゲノム配列を持ちながらも、糖尿病や高脂肪食など、親の健康状態、栄養状態が後に生まれる子供にも影響を与えうる可能性があります。私たちの研究室では、このようなエピジェネティックな遺伝情報の実体が何で
あるのか、それはどのように子供へ伝えられるのかといった分子機構の解明
に取り組んでいます。例えば、糖尿病によって精子DNAのメチル化状態が変
化します。これは、子供へ伝えられるエピジェネティック情報の有力な候補
の一つです。
エピジェネティックな機構による性決定システム

ヒトの場合、1対の性染色体があり、X染色体を2本持つとメスに、X染色体とY染色体を持つとオスになります。どちらの組み合わせを持つかは受精の時に遺伝的に決まります。ところが、性染色体を持たない動物もいます。カイガラムシは5対の染色体をもつ昆虫で、メスでもオスでも同じ組み合わせの10本の染色体(常染色体と言います)をもちます。メスは10本全てが活性化状態です。一方、発生の初期に1セット(5本)の染色体がエピジェネティックに不活性化されるとオスになります。一度、不活性化された染色体は生涯を終えるまで不活性化されたままです。しかも不活性化される染色体は全て父親から受け継いだ染色体であることが分かっています。この性決定に関わるエピジェネティックな分子機構について研究しています。




